Editorial : Valvulopathies asymptomatiques : importance de la Heart Valve Team
La prise en charge des patients asymptomatiques ayant une valvulopathie…

La prise en charge des patients asymptomatiques ayant une valvulopathie…
Pourquoi poser la question ? Parce que des auteurs anglais ont suggéré qu’il y avait une augmentation de l’incidence de l’endocardite infectieuse (EI) depuis que le NICE (National Institute for Health and Clinical Excellence) britannique a recommandé qu’il n’y ait plus aucune antibioprophylaxie lors de gestes à risque d’EI chez des cardiaques à risque d’EI.

Les valvulopathies médicamenteuses (VM) sont liées à un effet agoniste de certains médicaments sur les récepteurs cardiaques sérotoninergiques 5-HT2B. Le méthysergide, l’ergotamine, la fenfluramine, la dexfenfluramine, le pergolide, la cabergoline, le benfluorex et l’ecstasy sont aujourd’hui les substances inductrices identifiées.
Les VM sont à l’origine de fuites valvulaires essentiellement du cœur gauche, parfois associées à des sténoses, et sont caractérisées sur le plan anatomopathologique par une fibrose engainant les valves. Les atteintes polyvalvulaires sont fréquentes.
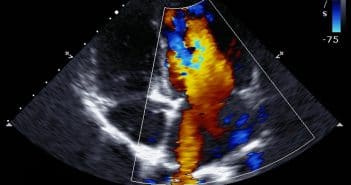
L’échocardiographie est l’examen diagnostique clé. Les signes typiques sont un épaississement valvulaire, une rétraction valvulaire et un mouvement valvulaire restrictif systolo-diastolique.
L’évolution est mal connue, avec possibilité de diminution, de stabilisation ou d’aggravation. Les formes frustes sont fréquentes. Les formes graves sont relativement rares et peuvent nécessiter une chirurgie valvulaire.
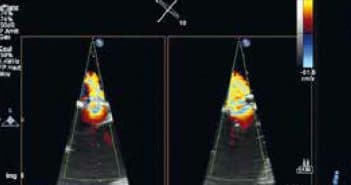
Malgré leur fréquence relativement élevée, la prise en charge des valvulopathies multiples est mal codifiée. Une bonne compréhension des mécanismes physiopathologiques et des conséquences ventriculaires gauches des valvulopathies isolées et de leur combinaison est nécessaire afin d’évaluer au mieux ces patients complexes.
L’évaluation de la géométrie ventriculaire gauche doit être systématique afin de détecter les signes d’une autre valvulopathie sévère associée à la valvulopathie princeps (par exemple, l’hypertrophie ventriculaire gauche excentrique liée à une insuffisance mitrale en cas de rétrécissement aortique).
La décision d’intervenir doit être prise au cas par cas chez ces patients complexes dans le cadre d’une évaluation spécialisée, au mieux dans un centre de référence pour l’évaluation des valvulopathies (“Heart Valve Clinic”).
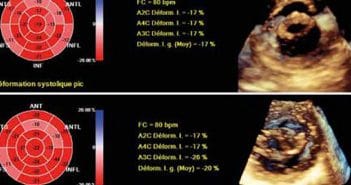
Le rétrécissement mitral (RM) est réputé être une valvulopathie avec un retentissement principalement d’amont et un ventricule gauche (VG) “protégé”. Cependant, nous savons depuis les années soixante-dix qu’il existe une dysfonction intrinsèque du VG liée au RM mais dont les mécanismes sont controversés. Ils associent une composante myocardique probable à des facteurs hémodynamiques en rapport avec le remodelage VG et la sévérité de la sténose.
Les techniques échographiques d’étude des déformations myocardiques ont montré que cette dysfonction existe chez tous les patients porteurs d’une sténose mitrale et qu’elle pourrait même devenir un paramètre pronostique et de suivi de ces patients.
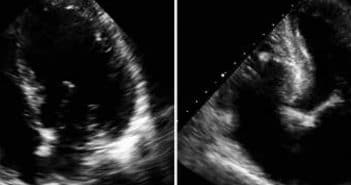
L’insuffisance aortique est un modèle d’augmentation de pré- et postcharge du ventricule gauche.
L’évaluation de la fonction et du remodelage ventriculaire gauche largement intriqués est un temps essentiel de l’écho-Doppler cardiaque chez le patient porteur d’une insuffisance aortique. Elle permet une évaluation à la fois de la sévérité et du pronostic de la valvulopathie.
Un remodelage extensif et/ou une altération de la fonction ventriculaire gauche ne doivent cependant pas faire contre-indiquer une intervention valvulaire pour un patient porteur d’une insuffisance aortique sévère car la chirurgie s’accompagne presque toujours d’une amélioration des conditions de charge.
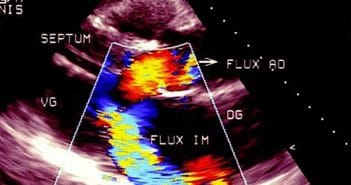
L’insuffisance mitrale (IM) est définie par le reflux systolique du sang du ventricule gauche vers l’oreillette gauche secondaire à un défaut d’étanchéité de la valve mitrale. Celui-ci peut être la conséquence d’une pathologie organique des feuillets mitraux et/ou de l’appareil sous-valvulaire mitral définissant les IM organiques ou primaires, ou bien la conséquence du remodelage et de la dysfonction systolique ventriculaire gauche (VG) d’origine ischémique ou non, sans anomalie anatomique de l’appareil mitral définissant les IM fonctionnelles ou secondaires, ischémiques ou non ischémiques. Nous aborderons ici le cas des IM primaires.
La dysfonction VG systolique est la complication redoutée de l’IM, caractérisée par une fibrose intermyocytaire et une diminution de la contractilité des myocytes de mécanismes mal connus ; sa détection précoce est difficile.
L’apparition d’une dyspnée d’effort, d’une fibrillation atriale, d’une diminution de la fraction d’éjection (FEVG), d’une augmentation du diamètre télésystolique VG ainsi qu’une élévation des pressions pulmonaires constituent autant de signaux chirurgicaux indiscutables mais tardifs dont la présence augmente la mortalité postopératoire.
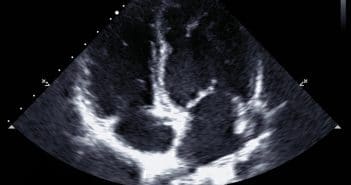
Le rétrécissement aortique calcifié (RAC) est la valvulopathie la plus fréquente. Dans le RAC serré, la présence de symptômes et/ou d’une fraction d’éjection ventriculaire gauche (VG) altérée est une indication d’intervention valvulaire aortique.
Les symptômes surviennent majoritairement avant que la fraction d’éjection du VG soit < 50 %. Ainsi, dès lors qu’elle est < 60 %, la baisse de la fraction d’éjection VG entraîne une mortalité post-intervention accrue. Il est donc important d’évaluer la fonction VG de façon plus fine et au-delà de la simple mesure de la fraction d’éjection.
L’évaluation échocardiographique de la fonction longitudinale à travers la mesure du strain longitudinal global (SLG) permet de rendre compte très précisément d’une altération myocardique longitudinale. Cela est particulièrement utile dans le contexte du RAC à bas débit-bas gradient (BDBG) et à fraction d’éjection préservée.
Dans le contexte du RAC BDBG et à fraction d’éjection altérée, l’évaluation de la fonction du VG sous dobutamine et l’appréciation de la présence de réserve contractile présentent un fort intérêt clinique et pronostique.
La prévalence des maladies valvulaires ne cesse de croître du…

L’anatomie de la valve tricuspide doit être analysée lors de toute échocardiographie. L’anneau tricuspide sera mesuré en diastole et en vue apicale 4 cavités.
L’anatomie du ventricule droit, et pas uniquement le TAPSE ou l’onde s’, doit être analysée systématiquement.
La fuite tricuspide reste un sujet thérapeutique difficile pour laquelle des innovations se profilent cependant. Nous détaillons ici quelques-uns des points clés à connaître.
